中国医疗器械标准管理年报(2021年度)
日期:2022-02-21 08:39:58 | 点击:
国家药监局坚持以习近平新时代中国特色社会主义思想为指导,把握新发展阶段,贯彻新发展理念,以推动高质量发展为主题,以规范管理为切入点,严格落实“最严谨的标准”要求,统筹推动医疗器械标准各项工作。
一、 做好标准体系顶层设计
2021年3月26日,国家药监局、国家标准委联合发布《关于进一步促进医疗器械标准化工作高质量发展的意见》(国药监械注〔2021〕21号,以下简称《意见》)。《意见》明确了到2025年基本建成适应医疗器械全生命周期管理需要,符合严守安全底线和助推质量发展高线新要求,与国际接轨、有中国特色、科学先进的医疗器械标准体系,实现标准质量全面提升,标准供给更加优质、及时、多元,标准管理更加健全、高效、协调,标准国际交流合作更加深入、更富成效的目标;提出了推进医疗器械标准化工作高质量发展的六大任务和三大保障措施。结合各领域“十四五”标准体系发展规划和监管实际,印发了《意见》任务分工,擘画了“十四五”期间医疗器械标准体系建设的顶层设计和标准化工作高质量发展的蓝图。
二、 健全标准组织架构
2021年,国家药监局整合各方资源,积极推动在监管急需领域、创新领域成立标准化技术组织,先后批准成立全国医疗器械临床评价、医用高通量测序2个标准化技术归口单位。
截至2021年12月31日,医疗器械标准化(分)技术委员会或技术归口单位[以下统称标委会(技术归口单位)]数量已增长到35个,包括13个总标委会(TC)、13个分标委会(SC)和9个技术归口单位,医疗器械标准组织架构见图1。
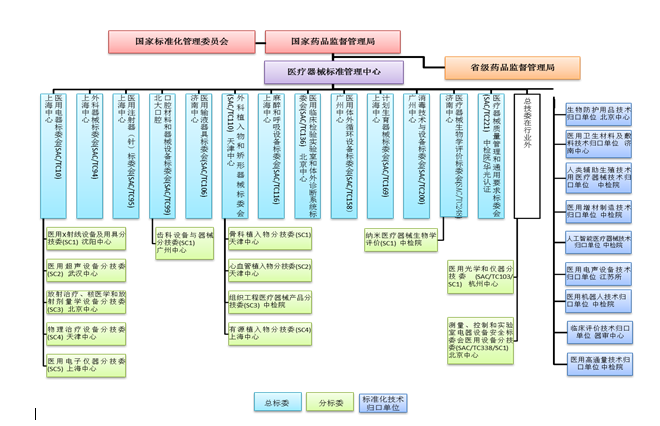
图1. 医疗器械标准组织架构图
指导全国外科植入物和矫形器械等4个标准化技术委员会换届和全国麻醉和呼吸设备等9个标委会委员调整。全国医用临床检验实验室和体外诊断系统标准化技术委员会(SAC/TC136)及全国医疗器械生物学评价标准化技术委员会 (SAC/TC248)2个标委会先后在国家标准委组织开展的全国专业标准化技术委员会考核评估中结果为一级。
三、 研制疫情防控标准
(一) 健全我国疫情防控标准体系
1.组织制定《新型冠状病毒核酸检测试剂盒质量评价要求》《新型冠状病毒抗原检测试剂盒质量评价要求》《新型冠状病毒抗体检测试剂盒质量评价要求》《新型冠状病毒IgM抗体检测试剂盒质量评价要求》《新型冠状病毒IgG抗体检测试剂盒质量评价要求》5项推荐性国家标准,已于2021年11月26日正式发布,从核酸、抗原及抗体检测为新型冠状病毒检测试剂的质量评价提供技术支撑。
2.结合疫情防控常态化管理的要求,以及医用防护产业发展的需求,组织 GB 19083-2010《医用防护口罩》和GB 19082-2009《医用一次性防护服》修订;组织制定正压防护服、传染病患者运送负压隔离舱等4项生物防护相关行业标准。
(二) 积极助力国际疫情防控
1.2021年8月30日,国际标准ISO 80601-2-90:2021《医用电气设备 第2-90部分:高流量呼吸治疗设备的基本安全和基本性能专用要求》,由国际标准化组织(International Organization for Standardization,ISO)和国际电工委员会(International Electrotechnical Commission,IEC)官网发布,这是由我国提出并负责完成的首个新冠肺炎疫情防控医疗器械国际标准项目。该标准的发布填补了此类产品国际标准的空白,为保障高流量呼吸治疗设备的安全有效,促进国际流通起到了积极作用,为全球疫情防控提供技术支持和贡献中国智慧。
2.积极参与国际标准技术规范ISO/TS 5798《通过核酸扩增方法检测新冠病毒的质量规范》制定工作,目前已进入工作组草案(WD)阶段。
3.组织制定的《医用防护口罩技术要求》等2项新冠疫情防控相关国家标准外文版已正式发布。
四、 优化评估强制性标准
2021年3月29日,为进一步优化医疗器械强制性标准体系,国家药监局综合司印发《医疗器械强制性标准优化工作方案》,确定了工作目标、总体要求,进一步明晰了医疗器械强制性标准和推荐性标准的范畴,以及标准修订、废止、转化的情形,明确了职责分工、进度安排和工作要求。
根据工作方案,拟转化为推荐性标准126项,转化为强制性国家标准14项,废止17项,修订(含整合)122项,保持继续有效179项(见图2),上述优化评估结果正在国家药监局网站公示。
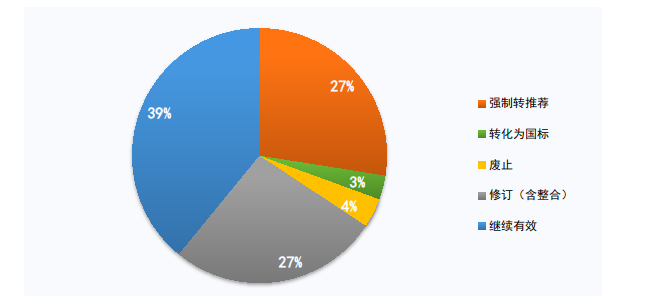
图2. 医疗器械强制性标准优化评估公示结果统计图
五、 完成标准制修订任务
2021年下达医疗器械国家标准制修订计划38项,医疗器械行业标准制修订计划79项;发布医疗器械国家标准35项,医疗器械行业标准146项,医疗器械行业标准修改单3项。截至2021年12月31日,医疗器械标准共计1849项(见表1),医疗器械标准体系持续优化。
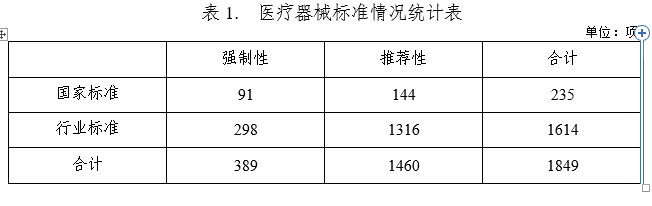
(一) 标准数量持续提升
2021年共发布医疗器械标准181项,标准发布数量较上一年度增长21%。近3年来,医疗器械标准发布数量稳步提升(见图3)。其中,国家标准发布数量增长显著。
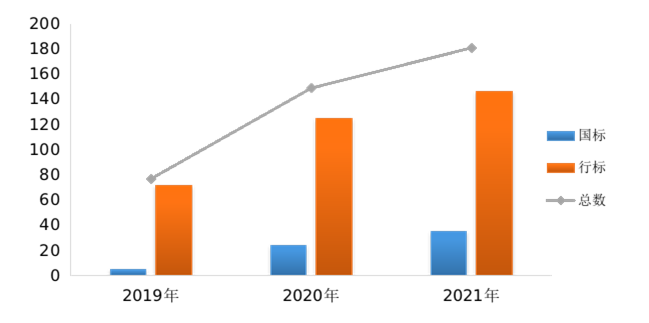
图3. 2019年—2021年医疗器械标准发布情况统计图
(二) 体系结构更加优化
截至2021年12月31日,按标准规范对象统计,现行有效的医疗器械标准中基础标准301项,占比16%;管理标准47项,占比3%;方法标准448项,占比24%;产品标准1053项,占比57%。
2021年发布的181项标准中,基础标准44项,占比24%;管理标准8项,占比4%;方法标准32项,占比18%;产品标准97项,占比54%。
重点支持基础通用和监管急需标准制定,2021年发布的35项国家标准中,18项为医用电气设备GB 9706.1配套的系列专用安全标准,5项为新冠病毒检测试剂质量评价要求标准,6项为临床检验医学实验室质量和能力要求系列标准,2项为医疗器械生物学评价系列基础通用标准,基础通用标准和疫情防控、监管急需标准占比达89%。
(三) 覆盖领域更加全面
截至2021年12月31日,按标准规范对象统计,现行有效的医疗器械标准按照《中国标准文献分类法》,主要归类在医疗器械综合(C30)至医用卫生用品(C48)之间,占比前5位的分别是:医用化验设备(C44)14%,矫形外科、骨科器械(C35)11%,一般与显微外科器械(C31)11%,口腔科器械、设备与材料(C33)10%,医用射线设备(C43)9%(见4)。医疗器械标准基本覆盖医用电气设备、手术器械、外科植入物等医疗器械各技术领域。
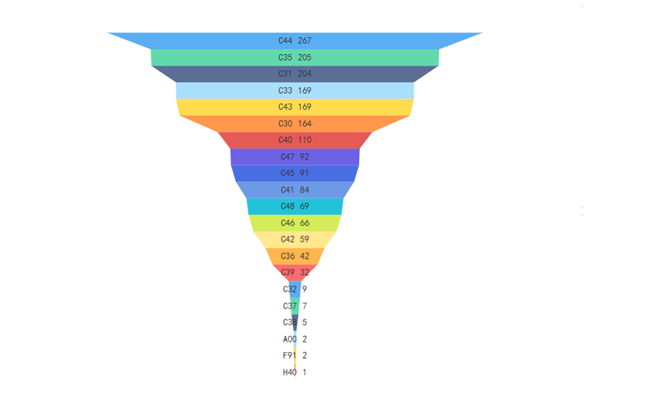
图4. 医疗器械标准各领域覆盖情况统计图(文献分类法)
2021年发布的181项标准中,发布数量排名前3的领域分别是医用化验设备(C44)、医疗器械综合(C30)、医用射线设备(C43),各领域发布标准数量见图5。
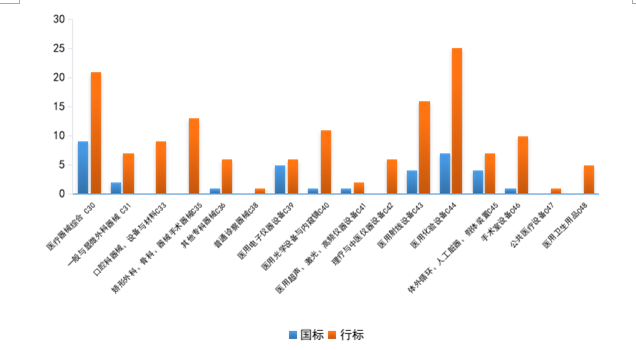
图5. 2021年发布医疗器械标准各领域分布情况统计图
推进急需标准快速制定,落实《意见》要求,对新兴产业等监管急需标准紧急立项、快速制定、及时发布。如加快组织制定发布《重组胶原蛋白》等产业监管急需标准。
(四) 标准效力得到增强
在对存量医疗器械强制性标准进行优化评估的基础上,进一步落实《意见》要求,将增量医疗器械强制性标准严格限定在涉及基本安全、性能要求,涉及安全的基础通用性技术要求和涉及《医疗器械安全和性能的基本原则》有关要求的范畴。2021年共发布医疗器械强制性标准41项,其中国家标准17项,行业标准24项。41项强制性标准中,34项为GB 9706.1配套的医用电气设备并列和专用安全标准,占比达83%;其余7项强制性标准中,有 2项强制性标准整合代替了原来的8项强制性标准。
六、 建立标准管理长效机制
(一) 优化标准制修订工作机制
鼓励企业、科研院所、社会团体等各相关方积极参与标准制修订工作。建立并完善标准信息化平台,在标管中心网站及时公开标准发布公告、计划通知、立项/委员征集信息等,标准制修订过程信息100%对外公开,引导各方积极参与标准制修订工作。
(二) 完善标准实施反馈机制
2021年国家药监局建立并运行医疗器械标准实施反馈机制,形成了标准制修订全链条闭环管理。
建立医疗器械标准意见反馈信息系统。自2021年7月1日起在标管中心网站运行,进一步健全了医疗器械标准实施反馈平台和沟通渠道。对公众反馈的标准实施意见,组织研究处理,做到条条有回复,件件有处理。
七、 参与国际标准制修订
(一)我国主导制定的2项国际标准正式发布
除由我国主导制定的首个新冠疫情防控相关医疗器械国际标准ISO 80601-2-90:2021外,首个由我国医疗器械行业标准(标准号:YY/T 1553-2017)转化的国际标准ISO 22679-2021《心血管植入物-心脏封堵器》于2021年11月正式发布。该国际标准的发布标志着我国医疗器械标准在持续提升与国际标准一致性程度的基础上,逐步开始探索将我国标准推广到国际。
(二)积极研提国际标准新项目
2021年共提出《计算机体层摄影设备的能谱成像 性能评价方法》《外科器械 吻合器 第1部分:术语和定义》《外科器械 吻合器 第2部分:通用要求》《胶原蛋白特征多肽定量测定方法标准》《脱细胞基质支架材料中残留DNA定量测定方法标准》等6项医疗器械国际标准立项申请。
(三)积极推进国际标准制定
我国主导制定的国际标准ISO 8536-15《医用输液器 第15部分:一次性使用避光输液器》目前处于最终国际标准草案(FDIS)投票阶段;国际标准ISO/DIS 24072《输液器进气器件气溶胶细菌截留试验方法》和技术规范ISO/TS 24560-1《组织工程医疗产品 软骨核磁评价 第1部分:采用延迟增强磁共振成像和 T2 Mapping技术的临床评价方法》已进入国际标准草案(DIS)阶段。
(四)积极参与国际标准化活动
组织参加国际标准化会议50余次,及时跟踪国际标准新动态,代表我国参与国际标准投票共计193次,新推荐16名专家成为国际标准组织注册专家,积极参与国际标准化活动。
八、 提升标准服务水平
一是按技术领域研究编印《医疗器械标准目录》,在国家药监局和标管中心网站面向社会公开。二是现行333项医疗器械强制性行标文本和871项非采标推荐性行标文本全部公开,提高标准可及性,服务标准各相关方。三是制定并公开医疗器械标准年度宣贯计划和通知,共组织对123项医疗器械标准进行宣贯培训。
九、 宣传推广标准理念
一是成功举办2021年“世界标准日”医疗器械标准化主题宣传活动。在北京举办“标准助推医疗器械高质量发展”为主题的首届中国医疗器械标准论坛活动,并组织医用X射线分标委在深圳举办了以“创新科技时代下的医疗器械标准”为主题的第七届IEC国际医疗器械标准论坛。
二是配合“2021年全国医疗器械安全宣传周”,组织举办医疗器械标准管理线上分会。解读最新医疗器械标准规划政策,讲解医用电气设备基础通用安全标准相关要求和实施要点,进一步宣传标准理念。
三是举办医疗器械标准综合知识培训班和GB 9706.1-2020免费线上公益培训班,5300余人参训,进一步统一认识、提高理解、促进标准顺利实施。
![]() 附表1.docx
附表1.docx
![]() 附表3.doc
附表3.doc
![]() 附表2.doc
附表2.doc
![]() 附表4.doc
附表4.doc
![]() 附表5.doc
附表5.doc
